-

'SK 최대주주' 이멕스팜 IMP5 공장 착공…2027년 가동 목표
[더구루=한아름 기자] SK그룹이 최대주주로 있는 베트남 제약사 이멕스팜(Imexpharm)이 현지에 전문의약품(의사의 처방전이 필요한 약) 공장을 짓는다. 생산 능력과 사업 영역을 확대해 시장 점유율을 높인다는 전략이다. 이멕스팜은 베트남 내 톱5위 규모 제약사다.
- 한아름 기자
- 2024-07-22 09:08
-

셀트리온·삼바에피스·LG화학, 'K바이오 3총사' 글로벌 톱10 진입…인도 시장 주목
[더구루=한아름 기자] 'K바이오 3총사'인 셀트리온과 삼성바이오에피스, LG화학이 글로벌 바이오시밀러(바이오의약품 복제약) 시장에서 존재감을 드러냈다. 인도 바이오시밀러 시장이 고성장함에 따라 이들의 성장 모멘텀에 대한 시장의 관심이 뜨겁다. 19일 글로벌 시장 조사기관 익스퍼트마켓리서치(Expert Market Research)에 따르면 셀트리온, 삼성바이오에피스, LG화학이 글로벌 바이오시밀러 시장을 선도하고 있는 톱10 기업으로 선정됐다. 인도 바이오시밀러 시장이 고성장하고 있어 이들의 행보에 더욱 관심이 쏠리고 있다. 익스퍼트마켓리서치는 인도 정부가 의료비 지출을 줄이기 위해 바이오시밀러 사용을 권장함에 따라 시장이 성장할 것으로 전망하며 이들 기업의 성장 모멘텀이 강하다는 진단을 내렸다. 셀트리온, 삼성바이오에피스, LG화학이 △화이자(Pfizer) △일라이릴리(Eli Lilly), 노바티스(Novartis) 등 글로벌 거대 제약사와 어깨를 나란히 했다는 점에서 유의미하다는 분석이 나온다. 이들은 특허가 만료됐거나 예정된 바이오시밀러를 개발하고 현지 규제당국에 허가 신청하면서 매출을 거둬들이고 있다. K바이오 3총사 중에서는 셀트리온이 가장 먼저
- 한아름 기자
- 2024-07-19 14:02
-

[단독] LG화학 美 아베오, 임상3상 미충족 속 틈새 기회 확보
[더구루=한아름 기자] LG화학 미국 손자회사 아베오 온콜로지(Aveo Oncology·이하 아베오)가 신세포암 치료제로 적응증 확대를 모색하던 약물 포티브다(성분명 티보자닙)가 임상 3상에서 실망스러운 성적표를 받아들였다. 아베오는 포티브다의 개발을 포기하지 않고 신세포암 치료제로서 가능성을 엿보겠다는 입장이다. 다만 아베오의 포티브다 적응증 확대 계획에 먹구름이 드리우게 되면서 LG화학에 악재로 작용할 것으로 전망된다. 19일 업계에 따르면 아베오가 포티브다와 브리스톨마이어스스큅(BMS) 면역항암제 '옵디보'(니볼루맙) 병용요법 관련 임상 3상 티니보-2(TiNivo-2)에서 유효성을 입증하는 데 실패했다. 무진행 생존기간(PFS) 연장이 나타나지 않아 주요 평가변수인 통계적 기준을 충족하지 못했다. 티니보-2는 면역관문억제제 치료 후 암이 진행된 진행성·재발성 또는 불응성 RCC환자를 대상으로 포티브다와 니볼루맙 저용량(0.89mg)을 병용 투여한 후 유효성·안전성을 확인하기 위해 기획됐다. 다만 아베오는 이번 연구에서 포티브다의 단독요법이 포티브다·옵디보 병용요법보다 치료효과가 높다는 점을 확인했다며 포티브다의 잠재력이 여전히 높다는 입장이다. LG화
- 한아름 기자
- 2024-07-19 10:12
-

[단독] 악재 겹친 대웅바이오, 중국서 항생제 수입·판매 중단 조치
[더구루=한아름 기자] 대웅 자회사 대웅바이오가 연이어 악재를 맞았다. 중국에서 공장 실사 거부 등 규정 위반으로 성남공장 항생제 수입·판매·사용 정지 처분을 받았다. 엎친데 겹친격으로 국내에선 약사법 등 규정 위반으로 식품의약품안전처로부터 일부 의약품에 대한 제조업무정치 처분을 받았다. 매출 공백 등 타격이 불가피할 전망이다. 19일 중국 국가약품감독관리국(NMPA)에 따르면 대웅바이오의 주사용 항생제 '뉴디짐주'(성분명 세포디짐 나트륨)를 공장 실사 거부 등 규정 위반으로 수입 통관을 중단 조치를 내렸다. 이번 조치에 따라 뉴디짐주는 중국 내에서 수입·판매·사용할 수 없게 됐다. 대웅바이오는 대웅의 원료의약품 전문 자회사다. NMPA는 "대웅바이오가 당국의 성남 공장 현장 실사를 수용할 수 없다는 입장을 밝혔다"며 "중화인민공화국약품관리법 99조, 해외 의약품·의료기기 실사에 관한 행정 조례 제 30조에 따라 대웅바이오가 수입 판매 요건을 충족하지 못한 것으로 판단한다"고 전했다. 이에 대웅바이오는 NMPA의 성남 공장 현장 실사를 거부한 이유는 현지에 누디짐주를 더이상 판매하지 않기로 결정한 데 따른 것이라는 입장을 내놨다. 대웅바이오 관계자는 "NMP
- 한아름 기자
- 2024-07-19 08:46
-
96%→82%…삼성에피스, '애브비 휴미라' 빈자리 꿰찬다
[더구루=한아름 기자] 바이오시밀러(바이오의약품 복제약)로 주춤한 휴미라 빈자리를 꿰차기 위해 삼성바이오에피스의 행보가 분주하다. 올해 초 미국 국가보훈부(VA)에 공급하는 입찰 계약을 단독으로 수주한 데 이어 상호교환성(IC·인터체인저블) 교체 처방 획득에 나서는 등 물밑경쟁이 치열해지고 있다.
- 한아름 기자
- 2024-07-17 08:58
-

한올바이오파마, 화이자 전 CBO '크리스토퍼' 영입
[더구루=한아름 기자] 대웅제약 계열사 한올바이오파마가 글로벌 대형 제약사 화이자(Pfizer) 출신의 최고사업개발책임자(Chief Business Development and Legal Officer)를 새로 영입했다. 신약 기술수출 등 상업화 분야에 새로운 피를 수혈해 안구건조증 치료제 'HL036'(성분명 탄파너셉트) 가치를 끌어올린다는 방침이다. 16일 업계에 따르면 한올바이오파마가 글로벌 사업에 드라이브를 걸기 위해 최고사업개발책임자 겸 법무책임자로 신규 사업 개발 전문가인 크리스토퍼 슬라빈스키(Christopher W Slavinsky) 박사를 영입했다. 슬라빈스키 박사는 바이오텍과 대형 제약사에서 25년 이상의 법률 및 사업 개발 경험을 보유했다. 슬라빈스키 박사는 지난 1989년 뉴욕주립대학교 스토니브룩(Stony Brook University)에서 생화학을 전공했으며, 토마스 제퍼슨 대학교(Thomas Jefferson University)에서 생화학 및 분자 생물학 석사를 수료한 후 워싱턴 대학교 로스쿨(Washington University in St. Louis School of Law)에서 법무박사(Juris Doctor) 학위를 취득
- 한아름 기자
- 2024-07-16 09:53
-
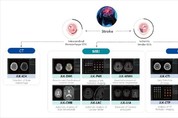
의료 AI 1호 상장기업 제이엘케이, 미국 시장 도전장
[더구루=한아름 기자] 국내 의료 인공지능(AI) 기업 제이엘케이가 뇌졸중 AI 기반 진단제품으로 미국 시장을 본격 공략한다. 제이엘케이는 지난 2019년 의료 AI 업계 최초로 코스닥에 상장된 기업으로, 한국인 뇌 MR(자기공명영상장치) 영상센터와 독점 계약을 통해 10년 이상 데이터를 공급받아 뇌졸중 관련 AI 전주기 솔루션 등을 개발하는 데 성공했다. 현재 확보한 100여개의 독보적인 원천 기술을 내세워 현지 시장에 성공적으로 안착한다는 목표다. 16일 미국 식품의약국(FDA)에 따르면 제이엘케이가 지난 5월 인허가 신청한 대혈관폐색 검출 AI 솔루션 'JLK-LVO' 등을 검토하고 있다. 오는 12월 승인 결정 여부를 발표할 예정이다. 현재 제이엘케이는 JLK-LVO 이에도 4개 솔루션을 인허가 신청하기 위한 준비 작업에 돌입한 상태다. 지난 4월 전립선암 AI 솔루션 메디허브의 인허가 승인을 획득한 데 이어 제이엘케이가 미국 의료 AI 시장 진출을 위해 본격 나섰다는 분석이 나온다. JLK-LVO는 혈관조영 CT(컴퓨터단층촬영) 이미지와 MR를 통해 대뇌혈관 폐색(LVO)을 신속하게 검출하는 AI 솔루션이다. 뇌경색 유형 분류 솔루션 'JBS-01K
- 한아름 기자
- 2024-07-16 09:01
-

광동제약, 글로벌 희귀의약품 4종 추가 도입 …伊 키에시와 계약
[더구루=이연춘 기자] 광동제약은 이탈리아 희귀의약품 전문기업 ‘키에시(CHIESI Farmaceutici)’의 희귀의약품 4종을 추가 도입하고, 국내에 독점 판매∙유통하는 계약을 체결했다고 15일 밝혔다. 이번 계약은 지난해 키에시로부터 ‘락손(Raxone)’, ‘엘파브리오(Elfabrio)’, ‘람제데(Lamzede)’ 총 3종의 희귀의약품을 도입한 데 이어 두 번째다. 이번 계약으로 도입된 품목은 말단비대증 치료제 ‘마이캅사‘(Mycapssa)’, 동형접합 가족성 고콜레스테롤혈증 치료제 ‘적스타피드(Juxtapid)’, 수포성 표피박리증 치료제 ‘필수베즈(Filsuvez)’, 지방이영양증 치료제 ‘마이알렙트(Myalept)’ 등 4종의 희귀질환 글로벌 신약이다. 마이캅사(Mycapssa)는 말단비대증 경구용 치료제다. 말단비대증은 뇌하수체에 종양이 생겨 성장호르몬이 과도하게 분비되는 희귀질환으로 기존에는 주사제로 평생 질환을 관리해야 했다. 마이캅사는 경구용 치료제로 개발되어 새로운 치료옵션이 필요했던 환자와 보호자에게 의미 있는 선택지를 제공한다. 적스타피드(Juxtapid)는 20세 이전 심장마비와 뇌졸중과 같은 심혈관 질환의 위험을 크게 증가시키는
- 이연춘 기자
- 2024-07-15 11:12
-

일진에스앤티, 加 오리니아에 주주서한…"이사회, 주주보호 역할 의문"
[더구루=한아름 기자] 일진그룹 바이오 신약 개발 계열사 일진에스엔티가 캐나다 제약사 오리니아(Aurinia)에 경영 정상화를 위한 행동에 나섰다. 오리니아에는 기업 본연의 역할에 집중해야 한다는 이유에서다. 일진에스티는 오리니아는 주주들의 의견을 존중하고 새로운 이사회를 구성하라고 요구했다.
- 한아름 기자
- 2024-07-15 09:35
-

씨젠, ‘AOGIN 2024’서 HPV 진단제품·PCR 기술 선봬
[더구루=이연춘 기자] 씨젠이 국제 학술대회에서 여성 자궁경부암의 원인으로 알려진 인유두종 바이러스(HPV) 진단제품의 우수성을 알리고 HPV 선별검사(screening test)의 중요성을 강조했다. 씨젠은 지난 11~13일 서울 중구 소공동 롯데호텔에서 열린 아시아·오세아니아 생식기 감염·종양학회(Asia-Oceania Research Organization in Genital Infection and Neoplasia, 이하 ‘AOGIN’)에 참가해 전시 부스를 운영하고 심포지엄 세션을 진행했다. AOGIN은 2004년 창립돼 아시아 및 오세아니아 25개국이 회원국으로 참여하는 학회로 여성 자궁경부암 치료와 예방에 관한 국제 학술대회를 개최하고 있다. 올해 서울에서 열린 AOGIN 2024에는 중국, 일본, 인도 등 총 22개국에서 전문가 500여 명이 참가해 HPV에 대한 최신 연구 결과와 임상경험을 교류했다. 씨젠은 사흘간 전시 부스에서 독자적인 정량 PCR 기술을 접목한 HPV 진단제품(Allplex™ HPV HR Detection·Allplex™ HPV28 Detection)을 선보였다. ‘Allplex™ HPV HR Detection’은 HPV
- 이연춘 기자
- 2024-07-15 08:28
-

대웅제약 나보타, K-톡신 최초 아르헨티나 '규제' 넘고 허가 획득
[더구루=이연춘 기자] 나보타가 국산 보툴리눔 톡신 최초로 아르헨티나 당국의 규제 허들을 넘었다. 대웅제약은 자사 보툴리눔 톡신 '나보타’가 지난달 아르헨티나 식품의약품의학기술청(ANMAT)으로부터 품목허가를 획득했다고 15일 밝혔다. 허가 용량은 100유닛과 200유닛이고 수출명은 '클로듀(CLODEW®)’다. 대웅제약은 아르헨티나의 높은 규제 허들을 넘고 국산 보툴리눔 톡신 제제로는 최초이자 유일하게 품목허가를 받았다. 이는 글로벌 시장에서 가장 권위 있는 미국 FDA와 유럽 EMA의 GMP 인증을 모두 받고 고품질 보툴리눔 톡신을 생산, 글로벌 시장에 판매하고 있기에 가능했다. 아르헨티나는 우리나라 제약사에게 진입 장벽이 매우 높은 시장이다. 아르헨티나가 정부가 인정하는 고위생감시국으로 분류되면 비교적 쉽게 의약품 품목허가를 받을 수 있지만, 우리나라는 아르헨티나 고위생감시국 리스트에 없다. 또 고위생감시국이 아니면 미국, 유럽 등 고위생감시국의 생산공장 GMP 인증도 필수적으로 보유해야 한다. 즉, 미국 FDA나 유럽 EMA의 인증이 없다면 진입 자체가 불가능한 시장이나 다름없다. 또한 아르헨티나는 매력적인 의약품 시장이기도하다. 아르헨티나는 중남미
- 이연춘 기자
- 2024-07-15 07:59
-
바이오젠·에자이, 알츠하이머병 치료제 '레켐비' 이스라엘서 승인…"6번째 허가"
[더구루=한아름 기자] 미국 바이오젠(Biogen)과 일본 에자이(Eisai)가 공동 개발한 알츠하이머 신약 '레켐비'(성분명 레카네맙)가 확산일로다. 이달에만 홍콩에 이어 이스라엘에서 품목허가를 받았다.
- 한아름 기자
- 2024-07-15 07:49
-
방산
안두릴·크라켄, '소형 USV 개발' 파트너십 체결
[더구루=홍성일 기자] 미국 인공지능(AI) 방산기업 안두릴 인더스트리(Anduril Industries, 이하 안두릴)가 영국 무인 함정 제작 기업 크라켄 테크놀로지 그룹(Kraken Technology Group, 이하 크라켄)과 소형 무인 수상정(USV) 개발을 위해 손잡았다. 양사는 기존 무인 함정 플랫폼에 자율주행 기술과 무기를 통합하는 방식으로 개발 속도를 끌어올려, 미국 해군 USV 도입 사업에 도전한다는 방침이다.

-
전자
TSMC, 3차원 SoIC로 반도체 성능 향상 전략 '재정비'
[더구루=정예린 기자] 대만 TSMC가 3차원(3D) 적층 기술 'SoIC(System on Integrated Chip)'를 중심으로 반도체 성능 향상 전략을 재정비했다. 유리 기판과 패널 기반 패키징 도입 시점을 늦추는 대신 검증된 적층·패키징 조합에 집중, 성능과 생산성을 동시에 확보할 수 있는 기반이 강화될 것으로 예상된다.