[더구루=김형수 기자] 삼성전자의 미국 의료기기 자회사 뉴로로지카(NeuroLogica)가 개발한 차세대 CT(컴퓨터 단층촬영) 관련 기술이 곧 미국 시장에서 본격적으로 사용될 전망이다.
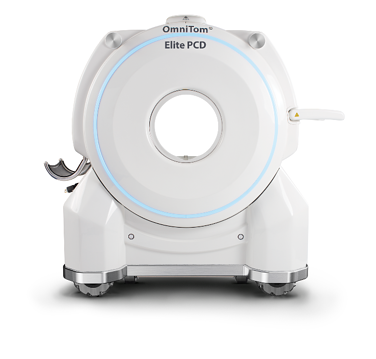
11일 업계에 따르면 미국 식품의약국(FDA)은 뉴로로지카의 모바일 CT 스캐너 옴니톰 엘리트(OmniTom Elite)의 광자계수검출기(Photon Counting Detector·PCD)에 대한 추가 510(k) 승인을 부여했다.
뉴로로지카는 FDA의 이번 결정에 따라 501(k) 승인을 획득한 최초의 단일 소스 광자계수 CT 스캐너를 시장에 공급할 수 있게 됐다고 전했다. 광자계수검출기와 짝을 이루는 단일 X레이 소스를 활용해 이미지 사이의 혼선 없이 변경 가능한 에너지 임계값으로 동시에 획득한 여러 세트의 CT 데이터를 생성할 수 있다는 설명이다.
이같은 기술을 활용하면 뼈, 혈전, 플라크, 두개내 종양(Intracranial Tumors) 등을 보다 정확하게 시각화하고 분할할 수 있다는 것이 뉴로로지카의 설명이다. 뉴로로지카는 필요한 투여량을 줄이는 것은 물론 주입하는 조영제 사용 방식을 근본적으로 바꿀 수 있는 가능성도 있을 것으로 내다보고 있다.
환자를 영상의학과로 보낼 필요없이 다용도의 실시간 모바일 이미징을 제공할 수 있는 능력을 갖춘 옴니톰 엘리트의 기능이 업그레이드된 셈이다. 뉴로로지카는 환자를 진단하고 치료를 시작하기까지 소요되는 시간을 더 단축할 수 있게 됐다고 전했다. 뉴로로지카는 현재 옴니톰 엘리트와 전체 모바일 CT 제품 라인을 미국 매사추세츠주 댄버스에서 생산하고 있다. FDA의 결정을 기다리는 동안 매사추세츠 종합병원에서 옴니톰 엘리트를 시범 운영하기도 했다.
데이비드 웹스터 뉴로로지카 COO는 "2004년 세계 최초의 다중 슬라이스 모바일 CT가 등장한 이후부터 현장 진단 이미징이 환자의 결과를 개선하고 외상적 사건 이후 삶의 질을 향상시킬 수 있다는 점을 알고 있었다"면서 "옴니톰 엘리트 플랫폼에 광자계수검출기를 도입함으로써 환자의 침대 옆에서 CT의 진단 가능성이 확장되길 바란다"고 말했다.

























